 Entenda o que aconteceu no caso CoronaVac
Entenda o que aconteceu no caso CoronaVac
Para entender o que aconteceu na suspensão dos testes da CoronaVac no Brasil é preciso conhecer as partes envolvidas num estudo clínico de vacinas e as responsabilidades de cada uma delas
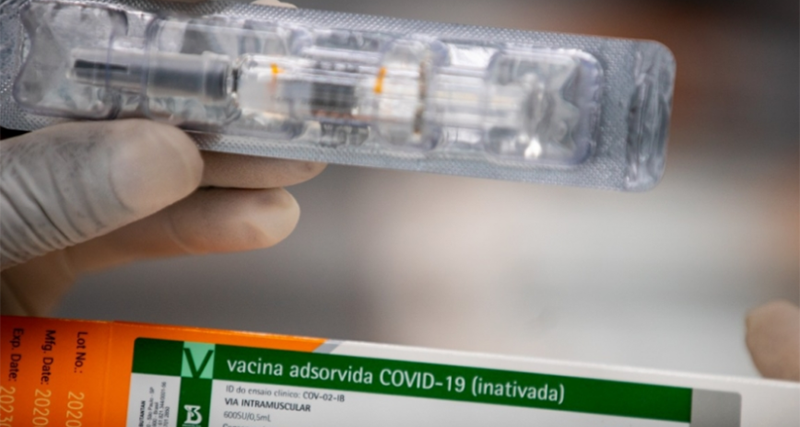
A vacina contra a covid-19 desenvolvida pela chinesa Sinovac está sendo testada no Brasil – Foto: Divulgação / Butantan
Para entender o que aconteceu na suspensão dos testes da CoronaVac no Brasil é preciso, primeiro, entender quais são as partes envolvidas num estudo clínico de vacinas e quais são as responsabilidades de cada uma delas.
Cada vacina tem um desenvolvedor e um patrocinador. O desenvolvedor é o agente — normalmente, uma empresa, universidade ou outro instituto de pesquisa — que inventou o produto. No caso da CoronaVac, esse agente é a Sinovac, uma empresa de biotecnologia chinesa que desenvolveu a vacina, utilizando uma versão inativada do vírus SARS-CoV-2 para induzir uma resposta imunológica protetora do organismo contra ele. O patrocinador é o agente que financia esse desenvolvimento tecnológico e/ou o estudo clínico do produto. No caso da CoronaVac, o patrocinador do estudo no Brasil é o Instituto Butantan, com recursos financeiros fornecidos pelo governo do Estado de São Paulo.
Para que o estudo possa ser realizado, ele precisa da autorização de duas agências reguladoras federais: a Comissão Nacional de Ética em Pesquisa (Conep) e a Agência Nacional de Vigilância Sanitária (Anvisa). A Conep avalia questões éticas relacionadas ao tratamento das pessoas envolvidas no estudo, enquanto que a Anvisa trata de questões relacionadas ao produto (envolvendo segurança, eficácia e qualidade) e seus potenciais impactos na população brasileira. Qualquer medicamento ou vacina só pode ser comercializado ou distribuído no País se tiver a aprovação da Anvisa — mesmo que seja uma distribuição gratuita, feita pelos órgãos públicos de saúde —, que é concedida (ou não) com base nos resultados do estudo clínico.
Os estudos clínicos de Fase 3 com vacinas costumam ser feitos em diversos centros, de diferentes países, envolvendo dezenas de milhares de participantes. Normalmente, cada um desses centros tem um pesquisador principal, responsável por conduzir o estudo e reportar seus resultados ao patrocinador, que, por sua vez, deve prestar contas periodicamente à Anvisa, à Conep e a um Comitê Independente de Monitoramento de Segurança (Data and Safety Monitoring Board – DSMB, em inglês), que é um grupo de especialistas independentes (sem vínculo direto com o projeto), incumbido de supervisionar a segurança do estudo.
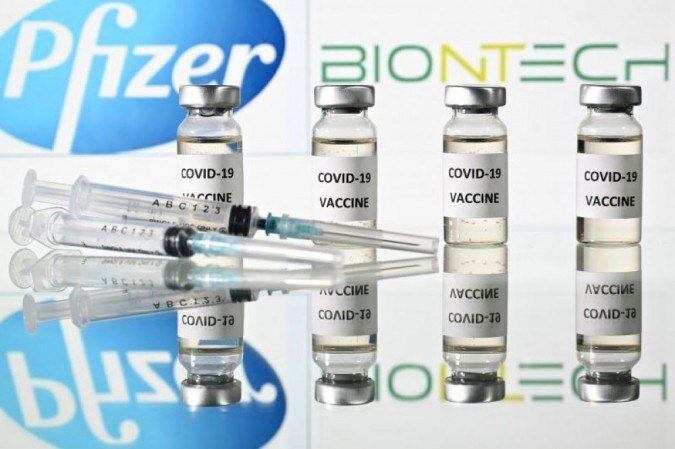 A farmacêutica Pfizer é a primeira a divulgar os resultados finais da terceira e última fase de testes clínicos de uma candidata a vacina para a covid-19. Desenvolvido em parceria com o grupo alemão BioNTech, o imunizante apresentou 95% de eficácia na prevenção à infecção pelo novo coronavírus,
A farmacêutica Pfizer é a primeira a divulgar os resultados finais da terceira e última fase de testes clínicos de uma candidata a vacina para a covid-19. Desenvolvido em parceria com o grupo alemão BioNTech, o imunizante apresentou 95% de eficácia na prevenção à infecção pelo novo coronavírus,

 As primeiras doses da vacina Coronavac chegaram ao Brasil nesta quinta-feira (19/11). O imunizante é produzido pelo laboratório chinês Sinovac. As 120 mil doses chegaram de avião, no Aeroporto de Guarulhos, em São Paulo, transportadas pela empresa Turkish Airlines.
As primeiras doses da vacina Coronavac chegaram ao Brasil nesta quinta-feira (19/11). O imunizante é produzido pelo laboratório chinês Sinovac. As 120 mil doses chegaram de avião, no Aeroporto de Guarulhos, em São Paulo, transportadas pela empresa Turkish Airlines. Parabéns ao Vereador Paulo Frange pela reeleição!
Parabéns ao Vereador Paulo Frange pela reeleição! Entenda o que aconteceu no caso CoronaVac
Entenda o que aconteceu no caso CoronaVac