- Escrito por Lilian Russo
- Imprimir
- Seja o primeiro a comentar!
Medicamento para hipertensão e controle de edemas pode causar câncer
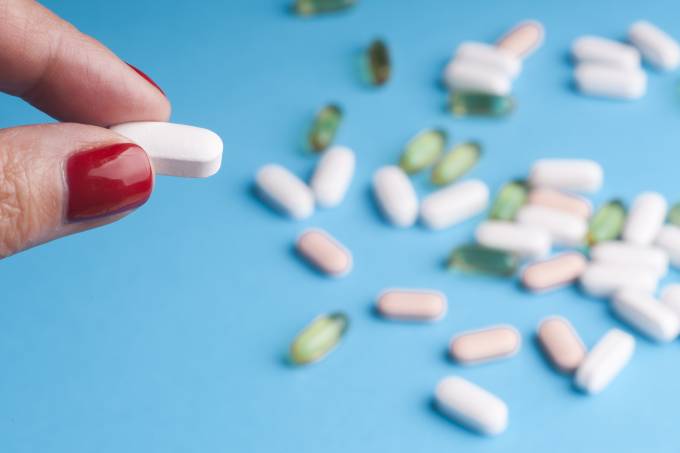 A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou hoje (4) um alerta para o aumento do risco de câncer de pele não-melanoma decorrente do uso cumulativo do medicamento hidroclorotiazida, utilizado para tratamento da hipertensão arterial e para controle de edemas.
A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou hoje (4) um alerta para o aumento do risco de câncer de pele não-melanoma decorrente do uso cumulativo do medicamento hidroclorotiazida, utilizado para tratamento da hipertensão arterial e para controle de edemas.
“A descoberta foi realizada por meio de estudos epidemiológicos que demonstraram uma associação dose-dependente cumulativa — que ocorre quando a dose utilizada de um determinado medicamento está
diretamente relacionada com seus efeitos — entre o medicamento em questão e o câncer de pele não-melanoma”, informou a Anvisa.
De acordo com a agência, em um dos estudos, foi possível notar também uma possível associação entre câncer de lábio e a exposição ao medicamento. “Ações fotossensibilizadoras da hidroclorotiazida, que facilitam a sua absorção pela pele, podem atuar como um possível mecanismo para a doença”.
A Anvisa considerou ainda as recomendações do Comitê de Avaliação de Riscos em Farmacovigilância da Agência Europeia de Medicamentos para classificar como plausível a associação entre o aumento do risco de câncer de pele não-melanoma e o uso em longo prazo de medicamentos contendo hidroclorotiazida.
Recomendações
Por meio de comunicado, a agência solicitou que os profissionais de saúde informem aos pacientes tratados com hidroclorotiazida sobre o risco de câncer de pele – sobretudo aqueles que já fazem uso do fármaco em longo prazo. Eles também devem ser orientados a verificar regularmente a pele quanto a novas lesões e a notificar imediatamente o profissional sobre qualquer tipo de lesão cutânea suspeita.
A orientação da Anvisa é que o tratamento não seja interrompido antes que os pacientes consultem o médico. “Lesões cutâneas suspeitas devem ser prontamente examinadas, incluindo exame histológico de biópsias. Medidas preventivas, tais como limitação da exposição à luz solar e aos raios ultravioleta, podem ser realizadas no intuito de minimizar o risco de câncer de pele. O uso de hidroclorotiazida pode ser revisto em pacientes com histórico de câncer de pele não-melanoma”.
A inclusão das novas informações de segurança nas bulas de todos os medicamentos que contêm o princípio ativo hidroclorotiazida será imediatamente solicitada pela agência.
Câncer de pele
O câncer de pele não-melanoma compreende os tumores mais comuns, que ocorrem principalmente em pessoas de pele clara, após exposição solar por longo tempo. Geralmente, apresentam apenas crescimento local, mas não cicatrizam ou se curam sem tratamento e tendem a aumentar com o tempo, podendo causar deformação, dor e sangramento.
Dados do Instituto Nacional do Câncer (Inca) indicam que esse é o tipo de câncer mais frequente no Brasil e corresponde a 30% de todos os tumores malignos registrados no país. Se detectado precocemente, a doença apresenta altos percentuais de cura. Entre os tumores de pele, o tipo não-melanoma é o de maior incidência e de mais baixa mortalidade.
Monitoramento
A Anvisa informou que monitora continuamente os medicamentos comercializados no Brasil e reforçou que profissionais de saúde e pacientes notifiquem os eventos adversos ocorridos com o uso de qualquer medicamento.
A comunicação de suspeitas de eventos adversos pelos pacientes pode ser feita por meio do formulário, pela Central de Atendimento ao Público (0800 642 9782) ou pela Ouvidoria (ouvidori@tende)
Para os profissionais de saúde, a Anvisa disponibiliza o sistema Notivisa em caso de notificação de eventos adversos.
Por Paula Laboissière - Repórter da Agência Brasil Brasília